Thiết bị ghi PR10-PR20-PR30 đáp ứng Chuẩn FDA 21 CFR Part 11
26/12/2021
Thiết bị ghi PR10-PR20-PR30 đáp ứng Chuẩn FDA 21 CFR Part 11 là một tiêu chuẩn được cục Quản lý Thực Phẩm và Dược phẩm Hoa kỳ ban hành có hiệu lực từ 20/8/1997,Thiết bị ghi của BrainChild đáp ứng chuẩn FDA21 CFR Part 11 được các nhà máy dược tin dùng để ghi và lưu lại dữ liệu trong các hoạt động của nhà máy
Thiết bị ghi PR10-PR20-PR30 đáp ứng Chuẩn FDA 21 CFR Part 11, đây là chuẩn được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ yêu cầu thiết bị phải đáp ứng khi dùng trong các nhà máy dược phẩm, thực phẩm, với tiêu chí nhằm mục đích bảo vệ cho con người
Thiết bị ghi PR10-PR20-PR30- đáp ứng tiêu chuẩn FDA 21 CFR Part 11
Thiết bị ghi PR10-PR20-PR30 đáp ứng Chuẩn FDA 21 CFR Part 11
Thiết bị PR được thiết kế để đáp ứng các tiêu chuẩn quy định trong CFR 21 phần 11 và nó được sử dụng như một phần của hệ thống đã được xác nhận.
1) Tất cả dữ liệu trong quá trình hoạt động được ghi lại bằng thiết bị PR được bảo vệ bằng “Chữ ký số” được mã hóa để đảm bảo tính xác thực của các bản dữ liệu đã ghi.
2) Bộ nhớ flash được sử dụng để cung cấp khả năng lưu trữ an toàn dữ liệu không phụ thuộc vào pin dự phòng và không chịu từ trường.
3) Phần mềm đánh giá tình hình xem lịch sử cung cấp khả năng xem các bản ghi dữ liệu và nhận dạng người có thể đọc được dữ liệu
4) ID người dùng và Mật khẩu được cung cấp sử dụng thiết bị để hạn chế quyền truy cập .
5) Tất cả các sự kiện hệ thống bao gồm thay đổi cấu hình, mất điện đều được ghi lại. Tất cả các mục nhập đều được đóng dấu thời gian và ngày tháng, bao gồm cả id nhà điều hành. Nhật ký đánh giá chi tiết đi kèm với tất cả dữ liệu quy trình được ghi lại bởi thiết bị PR10 / PR20 / PR30
Tất cả dữ liệu quy trình được ghi lại bằng thiết bị ghi PR10/PR20/PR30 đều ở định dạng độc quyền (chống giả mạo) và chỉ đọc từ giao diện người vận hành bình thường. Thông qua việc sử dụng phần mềm xem xét dữ liệu của Trình xem lịch sử, "chữ ký điện tử" có thể được thêm vào và kiểm tra để xác nhận tính toàn vẹn của dữ liệu. Nếu bất kỳ phần nào của bản ghi dữ liệu bị thay đổi, phần mềm Trình xem lịch sử sẽ cảnh báo người dùng về tính chất không hợp lệ của bản ghi.
Tất cả dữ liệu quy trình được ghi lại bằng thiết bị ghi PR10/PR20/PR30 đều ở định dạng độc quyền (chống giả mạo) và chỉ đọc từ giao diện người vận hành bình thường. Thông qua việc sử dụng phần mềm xem xét dữ liệu của Trình xem lịch sử, "chữ ký điện tử" có thể được thêm vào và kiểm tra để xác nhận tính toàn vẹn của dữ liệu. Nếu bất kỳ phần nào của bản ghi dữ liệu bị thay đổi, phần mềm Trình xem lịch sử sẽ cảnh báo người dùng về tính chất không hợp lệ của bản ghi.
Quy trình cho phép tuân thủ FDA 21 CFR Part-11 sử dụng trên thiết bị PR10/PR20/PR30.
#Bước 1: Bật nguồn,
#Bước 2: Vào menu- chọn Configuration menu
#Bước 3. Chọn instrument- từ menu configuration.
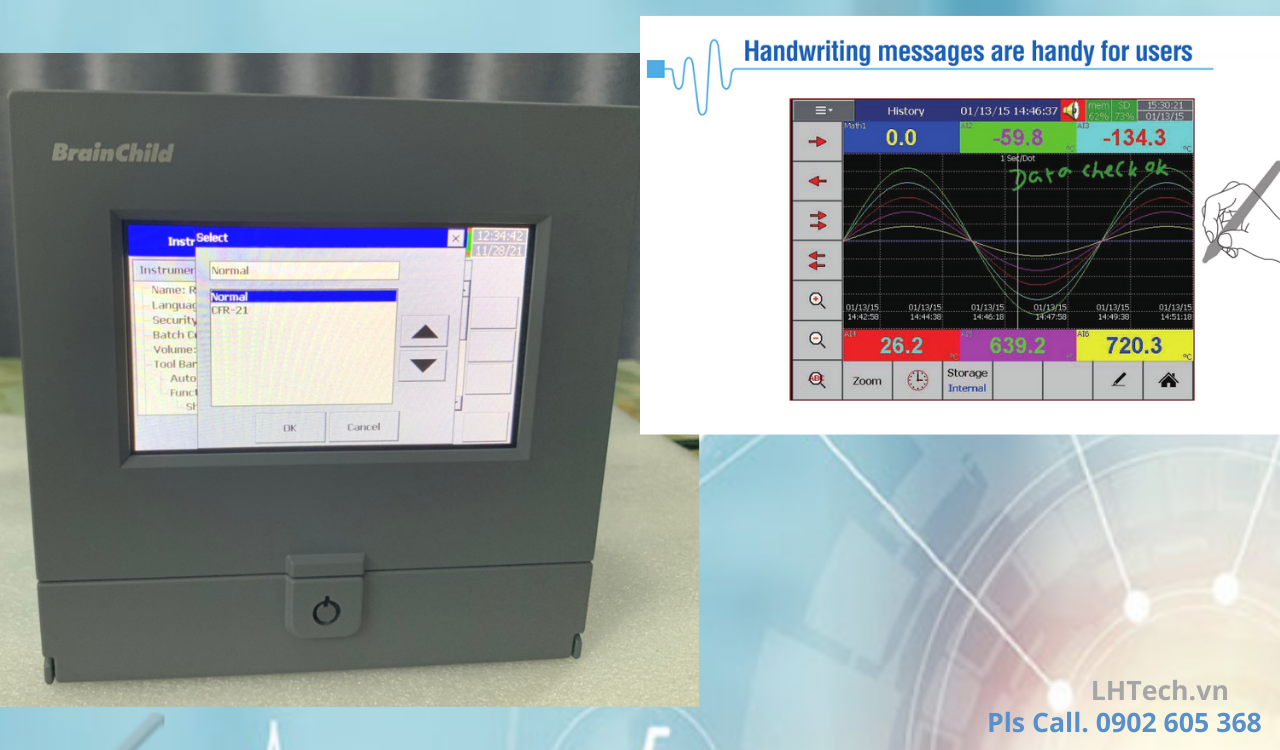
#Bước 4. Bật bật chế độ làm việc CFR-21.
#Bước 5. Thiết lập các tính năng đi kèm.
+/Logout: Thời gian logout user đang sử dụng.
+/Password validity: hiệu lực của mật khẩu.
+/Security level of functions: mức độ bảo mật của mật khẩu/ phân chia quyền hạn sử dụng cho từng tính năng.
+/Trong tài liệu (cũ) chia ra cấp bậc từ 1 đến 9, 9: quyền cao nhất, 1: là quyền thấp nhất.
+/Trong tài liệu ( mới) và thiết bị được thiết lập trên các quyền cho phép sử dụng hoặc không cho phép sử dụng. ( disable/ enable).
Sau khi chọn Back và Home thì phần cấu hình vừa thiết lập sẽ được lưu lại. Thiết bị ghi PR10/PR20/PR30 cần phải restarted- khởi động lại để thiết bị bật các thay đổi trên cấu hình sẽ kích hoạt FDA 21 CFR Part- 11.
Sau khi Khởi động lại thiết bị ghi cần được Đặt bằng Mật khẩu cho những người dùng cần thiết để truy cập.
Chọn Tên người dùng và Nhập Mật khẩu để Đăng nhập. Nếu đây là lần đầu tiên chọn người dùng thì Đầu ghi sẽ nhắc bạn đặt mật khẩu cho người dùng đó.
Sau khi Đăng nhập Chọn Menu Tài khoản Người dùng trong Menu Cấu hình để Tạo người dùng và chỉ định cấp độ Bảo mật của họ. Có thể tạo tối đa 30 người dùng..
Thủ tục ký hồ sơ:
1. Mở Phần mềm Trình xem Lịch sử trên PC
2. Tạo một dự án mới với việc lựa chọn loại ghi và đường dẫn tệp
3. Đăng nhập với Người dùng cụ thể và Mật khẩu đã được tạo trên Máy ghi âm để Kết nối với PC.
4. Sau khi Đăng nhập thành công Nhấn Yes ở Thông báo bên dưới để nhận Cài đặt cấu hình của Đầu ghi.
5. Đăng nhập bằng người dùng cụ thể và mật khẩu đã được tạo trên đầu ghi để kết nối với PC
6. Phần mềm Cấu hình sẽ nhận Cấu hình từ Máy ghi.
7. Bây giờ, hãy đóng phần mềm cấu hình để mở phần mềm xem lịch sử
8. Chọn Có để Lưu cấu hình
9. Đăng nhập với người dùng cụ thể và mật khẩu đã được tạo trên đầu ghi
10. Nhập dữ liệu đo tự động từ thiết bị ghi bằng cách nhấn Có trên Thông báo bên dưới
11. Dữ liệu đo được có thể được truy suất nhận thủ công từ thiết bị ghi bằng cách nhấp vào biểu tượng nhập
12. Kiểm tra tất cả các dữ liệu.
13. Sau đó nhấp vào Chữ ký trên thanh tác vụ có sẵn ở phía dưới cùng của màn hình trong trình xem lịch sử
14. Sau đó phần chữ ký sẽ hiện ra như sau
15. Theo mặc định, nút “Sign” sẽ bị tắt như hình trên. Sau khi dữ liệu mới nhất được nhập từ thiết bị ghi sang PC bằng Biểu tượng, khi đó nút “Ký” được bật. Bây giờ người dùng có thể ký hồ sơ với nhận xét của mình theo hình ảnh sau đây.
Trạng thái: Chọn Đạt / Không đạt
Nhận xét: Đưa ra nhận xét của bạn về dữ liệu đã kiểm tra
Sau đó nhấn “OK” để hoàn tất quá trình chữ ký tương đương với việc ký vào hồ sơ giấy.
FDA CFR21 Part 11 Section 11.10 (b)
Máy ghi không cần giấy có thể tạo các tệp dữ liệu quy trình trên bộ nhớ Kỹ thuật số an toàn (thẻ SD) hoặc trên Đĩa Flash USB ở định dạng độc quyền. Các tệp dữ liệu này được tạo từ các bản ghi an toàn được lưu trữ trong bộ nhớ flash trong. Các thuật toán phát hiện lỗi được sử dụng để đảm bảo rằng dữ liệu được lưu trữ đại diện trung thực cho các phép đo thô thực tế được thực hiện bởi máy ghi. Mỗi lần ghi vào phương tiện lưu trữ cũng được xác minh để đảm bảo tính toàn vẹn của bản ghi dữ liệu. Các tệp dữ liệu quy trình đã lưu trữ có thể được xem bằng phần mềm xem lại Trình xem lịch sử. Dữ liệu có thể được xem và in ở định dạng đồ họa. Các định dạng bảng tính tiêu chuẩn (ví dụ: Microsoft Excel) của các tệp dữ liệu đã lưu trữ có thể được tạo để người dùng không có phần mềm xem lại xem.
Dữ liệu lịch sử có thể được xem và in ở định dạng đồ họa như hình ảnh dưới đây.
Dữ liệu lịch sử và dữ liệu Sự kiện có thể được Xem và In ở định dạng Bảng tính Chuẩn như hình ảnh bên dưới
FDA CFR21 Part 11 Section 11.10 (c)
Máy ghi không giấy sử dụng bộ nhớ flash trạng thái rắn, để lưu trữ dữ liệu, dưới dạng thẻ Kỹ thuật số Bảo mật hoặc Đĩa Flash USB. Lưu trữ dữ liệu cho thiết bị này được quy định tối thiểu là 10 năm. Nó cung cấp khả năng lưu giữ dữ liệu năng lượng bằng 0, tức là tính toàn vẹn của dữ liệu không phụ thuộc vào pin dự phòng. Dữ liệu không bị ảnh hưởng bởi từ trường. Để lưu trữ dữ liệu lâu dài hơn nữa, các tệp lưu trữ có thể được sao chép vào CDROM hoặc vào máy chủ tệp mạng.
FDA CFR21 Part 11 Section 11.10 (d)
Máy ghi âm không cần giấy cung cấp khả năng giới hạn quyền truy cập vào cấu hình thiết bị và các chức năng quan trọng của người vận hành. Đối với mỗi người dùng, một id và mật khẩu duy nhất có thể được tạo để truy cập vào các thông số cấu hình. Id và mật khẩu có thể là chữ và số và độ dài tối đa 18 ký tự. Để có quyền truy cập vào các tham số cấu hình, cần nhập tổ hợp mật khẩu và id toán tử hợp lệ. Bất kỳ sửa đổi nào của cấu hình dụng cụ đều được ghi lại trong nhật ký đánh giá xác định người dùng chịu trách nhiệm về sự thay đổi. Máy ghi âm không sử dụng giấy sẽ tự động đăng xuất sau một khoảng thời gian không hoạt động trong vòng 10 phút.
FDA CFR21 Part 11 Section 11.10 (e)
Máy ghi không cần giấy tự động tạo ra một dấu vết kiểm tra thời gian được đóng dấu bao gồm mất điện và khôi phục, thay đổi cấu hình, kết xuất và xóa dữ liệu, các chức năng quan trọng của người vận hành. Thông tin này được lưu trữ trong nhật ký kiểm tra có thể được lưu trữ thành tệp vĩnh viễn trên thẻ Secure Digital hoặc trên USB Flash Disk. Nhật ký sự kiện / cảnh báo riêng biệt tự động tạo ra một bản ghi có đóng dấu thời gian về tất cả các thay đổi trạng thái cảnh báo và cũng có thể được lưu trữ thành một tệp vĩnh viễn.
FDA CFR21 Part 11 Section 11.10 (g)
Hệ thống bảo mật Máy ghi được nêu trong phần d) giới hạn quyền truy cập vào hệ thống để sửa đổi bất kỳ thông số cấu hình nào.
FDA CFR21 Part 11 Section 11.10 (h)
Lỗi hệ thống và trạng thái kênh đầu vào được ghi lại
FDA CFR21 Part 11 Section 11.10 (i)
Chỉ những người có trình độ phù hợp mới được tuyển dụng vào việc thiết kế & phát triển sản phẩm và việc đào tạo của họ được cập nhật để đáp ứng những tiến bộ trong công nghệ.
FDA CFR21 Part 11 Section 11.10 (k)
Hệ thống kiểm soát thiết kế được sử dụng được lập thành tài liệu đầy đủ và có thể truy xuất nguồn gốc. Tài liệu được cung cấp để cài đặt, cấu hình và vận hành trong Hướng dẫn sử dụng thiết bị.
FDA CFR21 Part 11 Sub Part C Section 11.300: Kiểm soát mã nhận dạng / mật khẩu
Mọi sự sao chép tên người dùng từ một tài khoản được tạo mới sẽ bị cấm.
Buộc người dùng nhập mật khẩu mới khi hết thời gian nhập mật khẩu.
Bất kỳ trường hợp đăng nhập không thành công nào sẽ được ghi lại để theo dõi kiểm tra.









Xem thêm